Xây dựng phương pháp định lượng linomycin và clindamycin trong nước thải bằng phương pháp LC MS MS
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (2.11 MB, 63 trang )
BỘ Y TẾ
TRƢỜNG ĐẠI HỌC DƢỢC HÀ NỘI
NGUYỄN LÊ NHẬT
MÃ SINH VIÊN: 1101377
XÂY DỰNG PHƢƠNG PHÁP ĐỊNH LƢỢNG
LINCOMYCIN VÀ CLINDAMYCIN
TRONG NƢỚC THẢI
BẰNG PHƢƠNG PHÁP LC-MS/MS
KHÓA LUẬN TỐT NGHIỆP DƢỢC SĨ
HÀ NỘI – 2016
BỘ Y TẾ
TRƢỜNG ĐẠI HỌC DƢỢC HÀ NỘI
NGUYỄN LÊ NHẬT
MÃ SINH VIÊN: 1101377
XÂY DỰNG PHƢƠNG PHÁP ĐỊNH LƢỢNG
LINCOMYCIN VÀ CLINDAMYCIN
TRONG NƢỚC THẢI
BẰNG PHƢƠNG PHÁP LC-MS/MS
KHÓA LUẬN TỐT NGHIỆP DƢỢC SĨ
Người hướng dẫn:
1. DS. Lê Xuân Kỳ
2. DS. Trần Thị Linh Anh
Nơi thực hiện:
1. Bộ môn Hoá phân tích – Độc chất
2. Bộ môn Vật lý – Hóa lý
HÀ NỘI - 2016
LỜI CẢM ƠN
Sau một thời gian thực hiện, khóa luận “Xây dựng phƣơng pháp định lƣợng
lincomycin và clindamycin trong nƣớc thải bằng phƣơng pháp LC-MS/MS” đã
đƣợc hoàn thành. Bên cạnh sự cố gắng của bản thân, em đã nhận đƣợc rất nhiều sự
khích lệ và giúp đỡ từ phía nhà trƣờng, bộ môn, gia đình và bạn bè.
Trƣớc tiên, em xin bày tỏ sự kính trọng và biết ơn sâu sắc tới DS. Lê Xuân Kỳ,
ngƣời thầy đã tận tình định hƣớng, chỉ bảo, đóng góp ý kiến quý báu cho em trong
suốt quá trình thực hiện và hoàn thành khoá luận.
Em xin gửi lời cảm ơn chân thành tới DS. Trần Thị Linh Anh, ngƣời đã trực
tiếp hƣớng dẫn và nhiệt tình giúp đỡ, hỗ trợ em trong suốt quá trình nghiên cứu,
thực hiện khoá luận.
Em cũng xin gửi cảm ơn tới các thầy cô, các anh chị kỹ thuật viên bộ môn Hóa
phân tích và Độc chất, bộ môn Vật lý - Hóa lý trƣờng Đại học Dƣợc Hà Nội đã giúp
đỡ và tạo điều kiện cho em rất nhiều trong thời gian thực hiện đề tài.
Cuối cùng em xin gửi lời cảm ơn gia đình, bạn bè là những ngƣời luôn động
viên, tạo động lực cho em trong suốt quá trình học tập và thực hiện khóa luận này.
Trong quá trình thực hiện, tuy đã nỗ lực và cố gắng hết mình nhƣng sẽ không
tránh khỏi những thiếu sót và sai sót, em rất mong sẽ nhận đƣợc những ý kiến chỉ
bảo, phê bình, góp ý từ phía các thầy cô để khoá luận của em tiếp tục đƣợc hoàn
thiện hơn.
Em xin trân trọng cảm ơn !
Hà Nội, ngày 12 tháng 05 năm 2016
Sinh viên
Nguyễn Lê Nhật
MỤC LỤC
ĐẶT VẤN ĐỀ ................................................................................................................. 1
CHƢƠNG 1: TỔNG QUAN.......................................................................................... 2
1.1. TỔNG QUAN VỀ ĐỐI TƢỢNG NGHIÊN CỨU.................................................. 2
1.1.1. Tổng quan về kháng sinh nhóm lincosamid .......................................................... 2
1.1.2. Một số đặc điểm của lincomycin .......................................................................... 3
1.1.3. Một số đặc điểm của clindamycin ......................................................................... 4
1.1.4. Tình trạng đề kháng của vi khuẩn với kháng sinh ................................................ 6
1.2. TỔNG QUAN VỀ CÁC PHƢƠNG PHÁP DÙNG TRONG NGHIÊN CỨU ....... 8
1.2.1. Phƣơng pháp sắc ký lỏng hiệu năng cao ............................................................... 8
1.2.2. Phƣơng pháp sắc ký lỏng hiệu năng cao ghép khối phổ ....................................... 8
1.2.3. Phƣơng pháp xử lý mẫu bằng kỹ thuật chiết pha rắn .......................................... 13
1.3. MỘT SỐ ĐỀ TÀI NGHIÊN CỨU ĐỊNH LƢỢNG CLINDAMYCIN VÀ
LINCOMYCIN TRÊN THẾ GIỚI................................................................................. 15
CHƢƠNG 2: ĐỐI TƢỢNG & PHƢƠNG PHÁP NGHIÊN CỨU .......................... 19
2.1. ĐỐI TƢỢNG & PHƢƠNG TIỆN NGHIÊN CỨU .............................................. 19
2.1.1. Hoá chất & thuốc thử .......................................................................................... 19
2.1.2. Thiết bị - dụng cụ ................................................................................................ 19
2.1.3. Đối tƣợng nghiên cứu .......................................................................................... 20
2.2. PHƢƠNG PHÁP NGHIÊN CỨU ......................................................................... 20
2.2.1. Phƣơng pháp thu thập, xử lý mẫu thô trƣớc khi tiến hành chiết tách ................. 20
2.2.2. Phƣơng pháp xử lý mẫu ...................................................................................... 20
2.2.3. Phƣơng pháp xây dựng quy trình định lƣợng lincosamid bằng HPLC MS/MS ........................................................................................................................... 21
2.2.4. Phƣơng pháp thẩm định quy trình phân tích đã xây dựng .................................. 22
2.3. PHƢƠNG PHÁP XỬ LÝ SỐ LIỆU ..................................................................... 24
CHƢƠNG 3: THỰC NGHIỆM VÀ KẾT QUẢ ........................................................ 25
3.1. XÂY DỰNG QUY TRÌNH PHÂN TÍCH ............................................................ 25
3.1.1. Khảo sát các điều kiện khối phổ ......................................................................... 25
3.1.2. Lựa chọn điều kiện sắc ký ................................................................................... 28
3.1.3. Lựa chọn điều kiện xử lý mẫu ............................................................................. 33
3.2. THẨM ĐỊNH PHƢƠNG PHÁP ........................................................................... 34
3.2.1. Độ thích hợp của hệ thống .................................................................................. 34
3.2.2. Độ đặc hiệu, độ chọn lọc của phƣơng pháp ........................................................ 35
3.2.3. Khoảng tuyến tính và đƣờng chuẩn .................................................................... 37
3.2.4. Độ độ đúng và độ lặp lại ..................................................................................... 39
3.2.5. Giới hạn phát hiện, giới hạn định lƣợng ............................................................. 40
4. CHƢƠNG 4: BÀN LUẬN ....................................................................................... 42
4.1. VỀ LỰA CHỌN KHÁNG SINH NGHIÊN CỨU ................................................ 42
4.2. VỀ PHƢƠNG PHÁP XỬ LÝ MẪU ..................................................................... 42
4.3. VỀ PHƢƠNG PHÁP PHÂN TÍCH ...................................................................... 43
4.4. VỀ THẨM ĐỊNH PHƢƠNG PHÁP ..................................................................... 44
KẾT LUẬN VÀ KIẾN NGHỊ........................................................................................ 45
TÀI LIỆU THAM KHẢO
PHỤ LỤC
DANH MỤC CÁC KÝ HIỆU, CHỮ VIẾT TẮT
Ký hiệu
AOAC
Tiếng Việt
Hiệp hội các nhà hoá phân tích
chính thống
Ion hoá học ở áp suất khí quyển
API
Tiếng Anh
Association of Official
Analytical Chemists
Atmospheric Pressure Chemical
Ionization
Atmospheric Pressure
Photoionization
Atmospheric Pressure Ionization
LIN
Lincomycin
Lincomycin
CLI
13
C3 TRI
DAD
ESI
IS
KS
HPLC
Clindamycin
13
C3Trimethoprim
Diode array detector
Electrospray Ionizaton
Internal standard
Clindamycin
13
C3Trimethoprim
Detector chuỗi diod
Ion hoá phun điện tử
Chuẩn nội
Kháng sinh
Sắc ký lỏng hiệu năng cao
APCI
APPI
HQC
LC MS/MS
MS
tR
Speak
MeOH
MQC
LOD
LOQ
LQC
PA
TB
TCCS
SPE
R(%)
SD
RSD
High performance liquid
chromatography
High quality control
Liquid chromatography Tandem Mass Spectrometry
Mass Spectrometry
Retention time
Area under the peak
Methanol
Middle quality control
Limit of Detection
Limit of Quantitation
Low quality control
Pure analysis
Solid Phase Extraction
Recovery
Standard Deviation
Relative Standard Deviation
Ion hoá bằng photon tại áp suất
khí quyển
Ion hoá áp suất khí quyển
Kiểm soát ở mức độ cao
Sắc ký lỏng ghép khối phổ hai lần
Khối phổ
Thời gian lƣu
Diện tích peak
Methanol
Kiểm soát ở mức độ giữa
Giới hạn phát hiện
Giới hạn định lƣợng
Kiểm soát ở mức độ thấp
Tinh khiết phân tích
Trung bình
Tiêu chuẩn cơ sở
Chiết pha rắn
Hiệu suất thu hồi
Độ lệch chuẩn
Độ lệch chuẩn tƣơng đối
DANH MỤC CÁC BẢNG
Bảng 1.1. Một số nghiên cứu định lƣợng kháng sinh lincomycin và clindamycin sử
dụng LC-MS/MS trên thế giới. .................................................................................15
Bảng 2.1. Các nguyên vật liệu dùng trong nghiên cứu .............................................19
Bảng 3.1. Các thông số hoạt động của nguồn ion hoá ..............................................27
Bảng 3.2. Điều kiện phân mảnh của từng kháng sinh và chuẩn nội .........................27
Bảng 3.3. Kết quả khảo sát độ thích hợp hệ thống ...................................................34
Bảng 3.4. Kết quả khảo sát khoảng tuyến tính và đƣờng chuẩn ...............................37
Bảng 3.5. Kết quả khảo sát độ đúng của phƣơng pháp (mức MQC) ........................39
Bảng 3.6. Kết quả giá trị LOD, LOQ của phƣơng pháp ...........................................41
DANH MỤC CÁC HÌNH
Hình 1.1. Công thức phân tử của lincomycin hydroclorid ..........................................3
Hình 1.2. Công thức phân tử của clindamycin hydroclorid ........................................4
Hình 1.3. Sơ đồ hệ thống thiết bị khối phổ .................................................................9
Hình 1.4. Sơ đồ tạo ion dƣơng bằng nguồn ESI .......................................................10
Hình 1.5. Sơ đồ cấu tạo thiết bị phổ kế tứ cực kiểu chập ba .....................................11
Hình 3.1. Kết quả khảo sát ion hóa tạo ion mẹ của LIN và CLI...............................26
Hình 3.2. Phổ đồ khảo sát ion con của các kháng sinh LIN, CLI và 13C3TRI ..........27
Hình 3.3. Sắc ký đồ khảo sát lựa chọn pha động ......................................................29
Hình 3.4. Sắc ký đồ phân tích các kháng sinh khi khảo sát thể tích tiêm mẫu .........31
Hình 3.5. Sắc ký đồ phân tích các kháng sinh khi khảo sát tốc độ dòng ..................33
Hình 3.6. Sắc ký đồ khảo sát độ đặc hiệu và chọn lọc của phƣơng pháp .................36
Hình 3.7. Đƣờng chuẩn giữa tỉ lệ SKS/SIS với nồng độ dung dịch lincomycin .........38
Hình 3.8. Đƣờng chuẩn giữa tỉ lệ SKS/SIS với nồng độ dung dịch clindamycin .......38
Hình 3.9. Sắc ký đồ xác định LOD, LOQ của phƣơng pháp ....................................40
1
ĐẶT VẤN ĐỀ
Tình trạng kháng kháng sinh đang gia tăng nghiêm trọng đe doạ lớn đến sức
khoẻ con ngƣời trên toàn thế giới. Các phƣơng pháp điều trị trƣớc đây sẽ không còn
hiệu quả và khi kháng sinh không còn hiệu lực, chỉ cần một vết thƣơng nhỏ bị
nhiễm trùng cũng có thể khiến ngƣời bệnh tử vong.
Việc sử dụng kháng sinh một cách ồ ạt, thiếu kiểm soát dẫn tới tình trạng vi
khuẩn kháng lại kháng sinh với mức độ ngày càng trầm trọng. Dƣ lƣợng kháng sinh
trong môi trƣờng là một trong những nguyên nhân của tình trạng kháng thuốc này.
Để giảm thiểu tình trạng kháng kháng sinh của vi khuẩn đồng nghĩa với việc
giảm thiểu việc đƣa kháng sinh ra ngoài môi trƣờng, giảm sự tiếp xúc giữa vi khuẩn
với kháng sinh. Do vậy, bên cạnh việc kiểm soát sử dụng kháng sinh chặt chẽ, đúng
cách, lƣợng kháng sinh thải ra môi trƣờng từ nƣớc thải y tế và công nghiệp dƣợc
phẩm cần phải đƣợc kiểm soát và hạn chế.
Trong những năm gần đây tại Việt Nam, số lƣợng và chủng loại kháng sinh
đƣợc sản xuất ngày càng nhiều, trong đó nhóm kháng sinh lincosamid là một trong
những nhóm có số lƣợng sản xuất và sử dụng tƣơng đối phổ biến. Vì vậy trong quá
trình sản xuất và sử dụng nhóm kháng sinh này, cần kiểm soát đƣợc dƣ lƣợng kháng
sinh thải ra môi trƣờng. Điều này đòi hỏi cần thiết phải xây dựng đƣợc một phƣơng
pháp định lƣợng có độ tin cậy để làm công cụ đánh giá.
Xuất phát từ những yêu cầu trên, chúng tôi đã tiến hành lựa chọn đề tài: “Xây
dựng phƣơng pháp định lƣợng kháng sinh lincomycin và clindamycin trong
nƣớc thải bằng phƣơng pháp LC-MS/MS”. Đề tài đƣợc thực hiện với 2 mục tiêu:
1. Lựa chọn được các điều kiện xử lý mẫu, điều kiện sắc ký lỏng khối phổ và xây
dựng được quy trình định lượng đồng thời hai kháng sinh lincomycin và
clindamycin trong nước thải bằng phương pháp LC-MS/MS.
2. Thẩm định được quy trình định lượng đã xây dựng.
2
1. CHƢƠNG 1: TỔNG QUAN
1.1. TỔNG QUAN VỀ ĐỐI TƢỢNG NGHIÊN CỨU
1.1.1. Tổng quan về kháng sinh nhóm lincosamid
Kháng sinh nhóm lincosamid bao gồm lincomycin, là một kháng sinh thiên
nhiên phân lập từ môi trƣờng nuôi cấy Streptomyces lincolensis và các dẫn xuất bán
tổng hợp gồm clindamycin và pirlimycin. Thế hệ kháng sinh này lần đầu tiên đƣợc
định hình trong những năm 1960 và hiện đang đƣợc sử dụng để điều trị một loạt các
bệnh nhiễm trùng. Phổ tác dụng của lincosamid chủ yếu đối với vi khuẩn gram
dƣơng, tuy nhiên cũng đƣợc sử dụng để chống lại vi khuẩn kỵ khí gram âm và các
sinh vật đơn bào. Cơ chế tác dụng của lincosamid là ngăn chặn sử tổng hợp protein
của vi sinh vật thông qua liên kết với các 23S rRNA của tiểu đơn vị 50S và bắt
chƣớc các trung gian đƣợc hình thành trong giai đoạn đầu của chu kỳ kéo dài. Các
lincosamid thƣờng đƣợc sử dụng để điều trị các nhiễm khuẩn do Streptococcus và
tụ cầu và đặc biệt hữu ích trong việc điều trị nhiễm khuẩn mô liên kết ở da, xƣơng
do khả năng hấp thu và tác dụng chống lại các chủng sản xuất độc tố hoại tử [25].
1.1.1.1. Cấu trúc nhóm lincosamid
Lincomycin có cấu trúc amid, tạo ra giữa acid 4-n-propyl hygric (acid 1- methyl
-4-propyl-2-pyrolidincarboxylic) với đƣờng amin có nhóm thế -SCH3 (methylthio).
Amino acid đóng vòng có tính base, tạo đƣợc muối với acid. Clindamycin đƣợc tạo
thành khi thay nhóm OH (7) của đƣờng amin của lincomycin bằng Cl, kèm theo
quay ngƣợc cấu hình C(7), có tính base nhƣ lincomycin [8].
1.1.1.2. Phổ tác dụng
Kháng sinh lincosamid nhạy cảm với Clostridium perfringens, Staphylococus
aureus nhƣng không nhạy cảm với vi khuẩn ruột Clostriduim difficile, nhạy cảm với
các chủng vi khuẩn yếm khí nói chung, loại nguồn gốc ruột và sinh dục nói riêng,
thuận lợi khi dùng lincosamid điều trị nhiễm khuẩn vùng bụng và chậu [7],[8].
1.1.1.3. Sự kháng thuốc của vi khuẩn
3
Vi khuẩn cũng kháng lại lincosamid. Có sự kháng chéo giữa lincosamid với các
kháng sinh cùng phổ tác dụng là macrolid và streptogramin (ngƣời ta còn nói
lincosamid, macrolid và streptogramin là các kháng sinh đồng loại) [7].
1.1.1.4. Tác dụng phụ
Viêm ruột kết màng giả khi dùng kháng sinh lincosamid. Nguyên nhân không
phải trực tiếp do kháng sinh mà do sự phát triển thuận lợi của chủng khuẩn ruột
Clostridium difficile không nhạy cảm với lincosamid, giải phóng lƣợng độc tố cao
gây viêm ruột. Hiện tƣợng này thƣờng gặp ở hơn đối với clindamycin [7],[8].
1.1.2. Một số đặc điểm của lincomycin
1.1.2.1. Công thức cấu tạo
Công thức: C18H34N2O6S.HCl.H2O
Phân tử lượng: 461,01g/mol [8].
.HCl.H2O
Hình 1.1. Công thức phân tử của lincomycin hydroclorid
Tên khoa học: Methyl 6,8-dideoxy-6-[[[(2S,4R)-1-methyl-4-propylpyrrolidin-2yl]amino]-1-thio]-D-erythro-α-D-galacto-octopyranosid hydroclorid [8].
1.1.2.2. Tính chất hóa lý
a) Tính chất vật lý
- Bột kết tinh màu trắng hoặc gần nhƣ trắng, vị đắng, hút ẩm.
- Rất tan trong nƣớc, dung dịch bền, khó tan trong ethanol 96%, rất khó tan
trong aceton và nhiều dung môi hữu cơ [6], [8].
b) Tính chất hóa học
- Phản ứng màu: sau khi thuỷ phân trong dung dịch HCl, tác dụng với natri
nitroprusiat và Na2CO3: xuất hiện màu đỏ tím (chung cho cả 2 chất)
- Dung dịch nƣớc cho phản ứng của ion Cl- [8].
1.1.2.3. Phổ tác dụng
4
Thuốc có tác dụng đối với nhiều vi khuẩn ƣa khí gram dƣơng, bao gồm các
Staphylococcus, Streptococcus, Pneumococcus, B. anthracis, C. diphtheriae, không
có tác dụng với Enterococcus.
Lincomycin có phổ tác dụng rộng đối với các vi khuẩn kỵ khí. Các vi khuẩn kỵ
khí gram dƣơng nhạy cảm bao gồm Eubacterium, Propionibacterium, Peptococcus,
Peptostreptococcus và nhiều chủng Clostridium perfringens và C. tetani.
Với liều cao, lincomycin có tác dụng đối với các vi khuẩn kỵ khí gram âm,
trong đó có Bacteroides spp. [7].
1.1.2.4. Chỉ định
Nhiễm khuẩn nặng do các vi khuẩn nhạy cảm, đặc biệt Staphylococcus,
Streptococcus, Pneumococcus ở ngƣời bệnh có dị ứng với penicilin nhƣ áp xe gan;
nhiễm khuẩn xƣơng do Staphylococcus; nhiễm khuẩn phụ khoa nhƣ nhiễm khuẩn ở
âm đạo, viêm màng trong tử cung, viêm vùng chậu; viêm màng bụng thứ phát; áp
xe phổi; nhiễm khuẩn huyết; mụn nhọt biến chứng và loét do nhiễm khuẩn kỵ khí.
Nhiễm khuẩn do các khuẩn đã kháng penicilin.
Nhiễm khuẩn ở các vị trí thuốc khác khó tới nhƣ viêm cốt tủy cấp tính và mạn
tính, các nhiễm khuẩn do Bacteroides spp [7].
1.1.3. Một số đặc điểm của clindamycin
1.1.3.1. Công thức cấu tạo
Công thức: C18H33ClN2O5S.HCl
Phân tử lượng: 461,47 g/mol [8].
.HCl
Hình 1.2. Công thức phân tử của clindamycin hydroclorid
5
Tên khoa học: Methyl 7-cloro-6,7,8-trideoxy-6-[[[(2S,4R)-1-methyl-4-propyl
pyrrolidin-2-yl]
carbonyl]
amino]-1-thio-L-threo-α-D-galacto-octopyranosid
hydroclorid [8].
1.1.3.2. Tính chất hóa lý
a) Tính chất vật lý
- Bột kết tinh trắng hoặc gần nhƣ trắng. Vị đắng nhẹ, hút ẩm.
- Dễ tan trong nƣớc, tan nhẹ trong ethanol; hầu nhƣ không tan trong dung môi
hữu cơ [8]
b) Tính chất hoá học
- Phản ứng màu: tƣơng tự lincomycin HCl [6], [8].
1.1.3.3. Phổ tác dụng
Tác dụng in vitro của clindamycin đối với các vi khuẩn sau đây:
Cầu khuẩn gram dƣơng ƣa khí: Staphylococcus aureus, Staphylococcus
epidermidis, Streptococcius (trừ S. faecalis), Pneumococcus.
Trực khuẩn gram âm kỵ khí: Bacteroides (B. fragilis) và Fusobacterium spp.
Trực khuẩn gram dƣơng kỵ khí không sinh nha bào: Propionibacterium,
Eubacterium và Actinomyces spp.
Cầu khuẩn Gram dƣơng kỵ khí: Peptococcus và Peptostreptococcus spp.,
Clostridium perfringens (trừ C. sporogenes và C. tertium). Các vi khuẩn khác:
Chlamydia trachomatis, Toxoplasma gondii, Plasmodium falciparum, Pneumocystis
carinii, Gardnerella vaginalis, Mycoplasma brominn.
Các loại vi khuẩn sau đây thƣờng kháng clindamycin: các trực khuẩn Gram âm
ƣa khí; Streptococcus faecalis; Nocardia sp; Neisseria meningitidis; Staphylococcus
aureus kháng methicillin; H. influenzae [7].
1.1.3.4. Chỉ định
Điều trị những bệnh nhiễm vi khuẩn nhạy cảm với clindamycin nhƣ B. fragilis
và Staphylococcus aureus, đặc biệt điều trị những ngƣời bệnh dị ứng với penicilin.
Clindamycin đƣợc dùng trong những trƣờng hợp sau:
- Phòng ngừa viêm màng trong tim, nhiễm khuẩn do cấy ghép phẫu thuật cho
ngƣời bệnh dị ứng với penicilin hoặc những ngƣời đã điều trị lâu bằng penicilin.
- Viên phổi sặc và áp xe phổi, nhiễm khuẩn đƣờng hô hấp nặng do các vi khuẩn
kỵ khí Streptoccocus, Staphylococcus và Pneumococcus.
6
- Nhiễn khuẩn trong ổ bụng nhƣ viêm phúc mạc và áp xe trong ổ bụng.
- Nhiễm khuẩn vết thƣơng mƣng mủ (phẫu thuật hoặc chấn thƣơng).
Vì có nguy cơ gây viêm đại tràng giả mạc nên clindamycin không phải là thuốc
đƣợc lựa chọn đầu tiên [7], [8].
1.1.4. Tình trạng đề kháng của vi khuẩn với kháng sinh
Báo cáo toàn cầu của WHO về tình trạng đề kháng kháng sinh năm 2014 đã chỉ
ra rằng việc các loại vi khuẩn biến đổi khiến cho các loại kháng sinh bị vô hiệu hoá
không còn là một dự đoán ở tƣơng lai mà đã trở thành hiện thực và đang diễn ra
trên toàn thế giới [26], [27].
Trên thế giới, nhiều chủng vi khuẩn gây bệnh đã trở nên ngày càng kháng thuốc
kháng sinh, các kháng sinh “thế hệ một” gần nhƣ không đƣợc lựa chọn trong nhiều
trƣờng hợp. Các kháng sinh thế hệ mới đắt tiền, thậm chí cả một số kháng sinh
thuộc nhóm “lựa chọn cuối cùng” cũng đang mất dần hiệu lực [12].
Vấn đề về thực trạng kháng kháng sinh đã mang tính toàn cầu và đặc biệt nổi
trội ở các nƣớc đang phát triển với sự tiến triển của các bệnh nhiễm khuẩn nhƣ
nhiễm khuẩn tiêu hoá, hô hấp, các bệnh lây truyền qua đƣờng tình dục, nhiễm
khuẩn bệnh viện... [5].
Tình trạng kháng kháng sinh ở Việt Nam đã ở mức độ cao. Trong số các nƣớc
thuộc mạng lƣới giám sát các căn nguyên kháng thuốc châu Á (ANSORP), Việt
Nam có mức độ kháng penicillin cao nhất (71,4%) và kháng erythromycin (92,1%)
[31]; 75% các chủng Pneumococci kháng với ba hoặc trên ba loại kháng sinh; 57%
Haemophilus influenzae kháng với ampicillin. Những năm 1990, tại thành phố Hồ
Chí Minh, chỉ có 8% các chủng Pneumococcus kháng với penicillin. Đến năm
1999-2000, tỉ lệ này đã tăng lên 56% [17]. Tình trạng kháng phổ biến ở các vi
khuẩn Gram âm. Theo kết quả nghiên cứu công bố năm 2009 cho thấy 42% các
chủng Enterobacteriaceae kháng với ceftazidim, 63% kháng với gentamicin và
74% kháng với nalidixic acid. Tỉ lệ kháng cao này đƣợc ghi nhận ở ngƣời khỏe
7
mạnh trong cộng đồng. Nhiều liệu pháp kháng sinh đƣợc khuyến cáo trong các tài
liệu hƣớng dẫn điều trị đã không còn hiệu lực [19].
Mặc dù khó đánh giá một cách định lƣợng nhƣng rõ ràng thực trạng kháng kháng
sinh đã, đang và sẽ gây ra những tác động tiêu cực đối với ngành y tế và kinh tế
Việt Nam.
Riêng đối với các kháng sinh nhóm lincosamid, tình trạng bị đề kháng bởi vi
khuẩn cũng không phải là ngoại lệ.
Trong nghiên cứu về sự kháng kháng sinh nhóm MLSB của Staphylococci đƣợc
phân lập ở Istanbul, Thổ Nhĩ Kỳ đăng trên tạp chí “The Journal of Microbiology”
năm 2007, Zerrin Aktas và các cộng sự đã chỉ ra rằng clindamycin thƣờng đƣợc sử
dụng để điều trị các bệnh nhiễm khuẩn trên da, mô mềm và xƣơng bởi khả năng
dung nạp thuốc tại các vị trí này, giá thành phù hợp, dạng đƣờng uống cũng nhƣ khả
năng thâm nhập vào các mô. Tuy nhiên đã có một số lƣợng lớn các báo cáo về thất
bại trong điều trị bằng clindamycin hoặc lincomycin trong các nhiễm khuẩn nghiêm
trọng do sự kháng kháng sinh nhóm MLSB của Staphyloccoci. Trong số 78 mẫu
bệnh phẩm chứa Staphylococci gram âm coagulase đƣợc đem thử độ nhạy cảm với
kháng sinh clindamycin thì chỉ có 42,1% còn nhạy cảm, trong khi đó có đến 55,9%
mẫu bệnh phẩm kháng lại kháng sinh ngay cả ở MIC90 [16].
Theo nghiên cứu “Cơ chế của sự kháng thuốc đối với nhóm kháng sinh macrolid
và lincosamid - Bản chất của các yếu tố kháng thuốc và ý nghĩa lâm sàng của
chúng” của Roland Leclercq, việc kháng kháng sinh nhóm macrolide và lincosamid
đang gia tăng nhanh chóng trong các báo cáo về các ca lâm sàng đƣợc phân lập có
chứa các vi khuẩn gram dƣơng, với các cơ chế kháng kháng sinh đa dạng bao gồm
thay đổi cấu trúc ribosom, bất hoạt thuốc và kết quả là tạo ra rất nhiều phenotype
kháng thuốc. Sự kháng thuốc không chỉ xuất hiện đối với chủng Staphylococci mà
còn xuất hiện trên Streptococci và Enterococci [24].
8
1.2. TỔNG QUAN VỀ CÁC PHƢƠNG PHÁP DÙNG TRONG NGHIÊN CỨU
1.2.1. Phƣơng pháp sắc ký lỏng hiệu năng cao
1.2.1.1. Khái niệm
Sắc ký lỏng hiệu năng cao (HPLC) là kĩ thuật phân tích dựa trên cơ sở của sự
phân tách các chất trên một pha tĩnh chứa trong cột, nhờ dòng di chuyển của pha
động lỏng dƣới áp suất cao. Sắc ký lỏng dựa trên cơ chế hấp phụ, phân bố, trao đổi
ion, loại cỡ, ái lực… tùy thuộc vào loại pha tĩnh sử dụng [3], [4].
1.2.1.2. Nguyên tắc
Mẫu phân tích đƣợc hòa tan trong dung môi và đƣợc cho qua cột bằng một
dòng chất lỏng liên tục (pha động). Các chất tan là thành phần của mẫu sẽ di chuyển
qua cột theo pha động với tốc độ khác nhau tùy thuộc vào hệ số phân bố giữa chất
tan với pha tĩnh và pha động. Nhờ tƣơng tác với pha tĩnh khác nhau nên tốc độ di
chuyển qua cột của các chất phân tích khác nhau, do vậy các thành phần của mẫu sẽ
tách riêng biệt thành dải, làm cơ sở cho phân tích định tính và định lƣợng.
1.2.2. Phƣơng pháp sắc ký lỏng hiệu năng cao ghép khối phổ
Phƣơng pháp sắc ký lỏng hiệu năng cao ghép nối với khối phổ là phƣơng pháp
phân tích dụng cụ quan trọng và đƣợc sử dụng rộng rãi hiện nay để phân tích thành
phần và cấu trúc các chất với khả năng xác định hàm lƣợng siêu vết, giới hạn phát
hiện có thể lên đến 10-14 gam [3].
Về cơ bản, sắc ký lỏng khối phổ là phƣơng pháp sắc ký lỏng hiệu năng cao
(HPLC) sử dụng detector khối phổ. Sau khi loại bớt tạp chất, ion hoá và tách ra từ
cột sắc ký, các chất phân tích đi vào thiết bị khối phổ. Trong thiết bị khối phổ, các
chất đƣợc chuyển sang trạng thái bay hơi, sau đó đƣợc ion hoá bằng các phƣơng
pháp thích hợp. Các ion tạo thành đƣợc đƣa vào bộ phận phân tích khối, tại đây các
ion sẽ đƣợc tách thành từng phần riêng biệt nhờ vào tác dụng của điện trƣờng hoặc
từ trƣờng dựa trên số khối m/z khác nhau và cuối cùng đi đến bộ phận phát hiện và
xử lý số liệu. Hình 1.3 mô tả sơ đồ hệ thống thiết bị khối phổ.
9
Hình 1.3. Sơ đồ hệ thống thiết bị khối phổ
1.2.2.1. Thiết bị khối phổ
Một thiết bị khối phổ bao gồm các bộ phận chính nhƣ sau:
a) Bộ nạp mẫu (inlet)
Chuyển các mẫu cần phân tích vào nguồn ion hoá của thiết bị khối phổ. Trong
sắc ký lỏng khối phổ, bộ phận nạp mẫu chính là đầu ra của cột sắc ký. Mẫu ở dạng
lỏng hoặc rắn sẽ đƣợc chuyển sang dạng hơi bằng các phƣơng pháp thích hợp để tạo
ra sự tƣơng thích giữa hệ thống sắc ký lỏng và đầu dò khối phổ. Đầu dò khối phổ
đòi hỏi mức độ chân không cao, nhiệt độ cao, các chất khảo sát phải ở trạng thái
khí, vận tốc dòng chảy nhỏ, trong khi hệ thống LC lại hoạt động ở áp suất cao với
một lƣợng dung môi tƣơng đối lớn, nhiệt độ tƣơng đối thấp, các chất phân tích ở thể
lỏng. Kỹ thuật ion hóa tại áp suất khí quyển (API) ra đời đã giải quyết đƣợc vấn đề
này và tạo ra bƣớc đột phá thật sự cho phƣơng pháp LC-MS/MS.
b) Bộ nguồn ion hóa (ion source)
Tại đây các phân tử ở trạng thái hơi bị bắn phá tạo ra ion phân tử hoặc các ion
mảnh, mỗi ion có khối lƣợng m và điện tích z nhất định. Tỉ số m/z (số khối) của
mỗi ion là một thông số quan trọng mà nhờ nó, bộ phận phân tích khối có thể tách
riêng đƣợc các ion này.
Có ba kiểu hình thành ion: ESI, APCI, APPI. Trong nghiên cứu này, chúng tôi
sử dụng máy phân tích với bộ phận ion hóa bằng kỹ thuật ESI để ion hoá các phân
tử trung hoà thành các ion phân tử, các mảnh ion hoặc các gốc mang điện tích. Đây
là kỹ thuật ion hóa đƣợc ứng dụng cho những hợp chất không bền nhiệt, phân cực,
có khối lƣợng phân tử lớn và đƣợc xem là kỹ thuật ion hóa “êm dịu” hơn APCI,
thích hợp cho phân tích các hợp chất sinh học nhƣ protein hoặc các polyme.
10
ESI đƣợc thực hiện ở áp suất khí quyển. Tại đầu ống dẫn mao quản, dƣới ảnh
hƣởng của điện thế cao và sự hỗ trợ của khí mang, mẫu đƣợc phun thành những hạt
sƣơng nhỏ mang điện thích tại bề mặt. Khí ở xung quanh các giọt này tạo nhiệt
năng làm bay hơi dung môi ra khỏi giọt sƣơng. Đến một giới hạn, các hạt sƣơng bị
phân chia thành những hạt nhỏ hơn vì lực đẩy lúc này lớn hơn sức căng bề mặt. Quá
trình này đƣợc lặp lại nhiều lần để hình thành những hạt rất nhỏ. Sau đó các ion
phân tích đƣợc chuyển thành thể khí bởi lực đẩy tĩnh điện rồi sau đó đi vào bộ phận
phân tích khối.
Hình 1.4. Sơ đồ tạo ion dương bằng nguồn ESI
c) Bộ phận phân tích khối (mass analyzer)
Sau khi đƣợc tạo thành thì các ion sẽ đƣợc gia tốc và tách riêng theo tỷ số m/z
nhờ tác dụng của điện trƣờng và từ trƣờng để đi đến bộ phận phát hiện.
Một số bộ phân tích khối thƣờng dùng: tứ cực (quadrupole), bẫy ion (ion trap),
ống đo thời gian bay (time-of-flight tube).
Bộ phân tích khối tứ cực chập ba đƣợc sử dụng phổ biến trong kỹ thuật LCMS/MS và đây cũng là kỹ thuật đƣợc chúng tôi sử dụng trong nghiên cứu này. Bộ
phận phân tích khối tứ cực có 4 thanh tích điện đặt song song, 2 thanh đối nhau có
điện tích bằng nhau. Khi một trƣờng điện từ đƣợc tạo ra bằng sự kết hợp giữa dòng
một chiều (DC) và điện thế tần số (RF) cao, các ion chuyển động trong nó sẽ dao
động phụ thuộc vào tỉ số m/z và trƣờng RF. Chỉ có những ion có tỉ số m/z phù hợp
mới có thể đi qua đƣợc bộ lọc này. Các ion phù hợp với tần số quét sẽ đi thẳng tới
detector, những ion khác bị phá hủy do bị va đập vào tứ cực.
11
Bộ phân tích tứ cực chập ba gồm 3 tứ cực xếp nối tiếp nhau Q1, Q2, Q3 để ghi
phổ. Ttứ cực thứ nhất (Q1) có nhiệm vụ tách các ion, lựa chọn ion mẹ với m/z nhất
định từ nguồn ion chuyển đến để chuyển đến Q2. Ở tứ cực thứ 2 (Q2) với áp suất
cao, các ion phân tử bị phân li do va chạm với khí trơ có mặt nhƣ khí N2, Ar, He.
Sau đó tất cả các ion con đƣợc chuyển qua bộ tách Q3, có nhiệm vụ tách các ion
đƣợc chuyển từ Q2, để tới bộ phận phát hiện. Kỹ thuật phân tích khối phổ kiểu này
đƣợc gọi là khối phổ hai lần MS/MS và thƣờng đƣợc dùng để khẳng định cấu trúc
các chất hữu cơ và phân tích hỗn hợp nhiều thành phần.
Hình 1.5. Sơ đồ cấu tạo thiết bị phổ kế tứ cực kiểu chập ba
d) Bộ phận phát hiện ion (detector)
Có hai loại bộ phận phát hiện phổ biến: bộ phận phát hiện nhân electron
(electron multiplier) và bộ phận phát hiện nhân quang (photomultiplier). Bộ phận
phát hiện nhân electron là một trong những detector phổ biến nhất, có độ nhạy cao.
Các ion đập vào bề mặt dinod làm bật ra các electron. Các electron thứ cấp sau đó
đƣợc dẫn tới các dinod tiếp theo và sẽ tạo ra electron thứ cấp nhiều hơn nữa, tạo
thành dòng các electron. Bộ phận phát hiện nhân quang cũng giống nhƣ thiết bị
nhân electron, các ion ban đầu đập vào một dinod tạo ra dòng các electron. Khác
với detector nhân electron, các electron sau đó sẽ va đập vào một màn chắn
phospho và giải phóng ra các photon. Các photon này đƣợc phát hiện bởi một bộ
nhân quang hoạt động nhƣ thiết bị nhân electron. Các ống nhân quang đƣợc đặt
trong chân không nên loại bỏ đƣợc các khả năng nhiễm bẩn.
e) Bộ phận ghi và xử lý số liệu (data system)
Là một hệ thống bao gồm hệ thống kết nối và thu nhận dữ liệu thô và phần
12
mềm kiểm soát, điều khiển thiết bị, quá trình phân tích và tính toán, xử lý, báo
cáo, kết xuất dữ liệu thô vừa thu đƣợc.
1.2.2.2. Một số kỹ thuật ghi phổ
Trong phân tích khối phổ việc xác định chính xác 1 ion rất quan trọng cho việc
xác định đƣợc hợp chất cần phân tích. Một hợp chất xác định trong những điều kiện
nhất định sẽ cho 1 ion có số khối xác định trên phổ đồ. Tuy nhiên, một ion có số
khối xác định trên phổ đồ lại có thể xuất phát từ nhiều hợp chất khác nhau vì vậy
trong phân tích một hỗn hợp hoặc lẫn nhiều tạp chất nếu điều kiện sắc kí chƣa đảm
bảo việc phân tách thì việc nhận định các ion thông qua số khối tên phổ đồ có thể bị
ảnh hƣởng. Đối với trƣờng hợp này khối phổ 1 lần (MS) có thể cho kết quả không
chính xác so với kỹ thuật khối phổ nhiều lần (2 lần MS/MS).
a) Quét toàn phổ (Full Scan)
Khi thao tác với chế độ scan, đầu dò sẽ nhận đƣợc tất cả các mảnh ion để cho
khối phổ toàn ion đối với tất cả các chất trong suốt quá trình phân tích. Thƣờng
dùng để nhận danh hay phân tích khi chất phân tích có nồng độ đủ lớn. Đối với đầu
dò khối phổ ba tứ cực, chế độ Full scan MS thƣờng đƣợc lựa chọn để khảo sát ion
mẹ, chế độ Full scan MS/MS quét tất cả các ion con tạo thành thƣờng đƣợc sử dụng
để xác định ion con cho tín hiệu ổn định và bền nhất.
b) Selected Ion Monitoring (SIM)
Trong chế độ SIM, đầu dò MS chỉ ghi nhận tín hiệu một số mảnh ion đặc trƣng
cho chất cần xác định và cho tín hiệu của các ion đã đƣợc lựa chọn trƣớc đó, do vậy
không thể dùng để nhận danh hay so sánh với các thƣ viện có sẵn. Chế độ SIM
thƣờng đƣợc lựa chọn để khảo sát năng lƣợng phân mảnh khi đã biết ion mẹ.
c) SR
Selected Reaction
onitoring và
R
ultiple Reaction
onitoring
Đối với máy khối phổ tứ cực chập ba, 2 kỹ thuật ghi phổ có độ nhạy cao thƣờng
đƣợc sử dụng là SRM và MRM.
- SRM: cô lập ion cần chọn, sau đó phân mảnh ion cô lập đó, trong các mảnh ion
sinh ra, cô lập 1 mảnh ion con cần quan tâm và đƣa vào đầu dò để phát hiện.
13
- MRM: cô lập ion cần chọn (ion mẹ) ở tứ cực thứ nhất, phân mảnh ion cô lập đó
tại tứ cực thứ 2 (thực chất là buồng va chạm) thu đƣợc các ion con, cô lập 2 (hoặc
nhiều) ion con cần quan tâm ở tứ cực thứ 3 và đƣa vào đầu dò để phát hiện [2], [11].
1.2.2.3. Một số ưu điểm của sắc ký lỏng khối phổ
LC-MS có tính chọn lọc và độ nhạy cao, thƣờng đƣợc sử dụng để xác định
lƣợng siêu vết trong mẫu có thành phần phức tạp nhƣ định tính, định lƣợng thuốc và
các dạng chuyển hóa trong dịch sinh học, độc chất học, định lƣợng dƣ lƣợng thuốc
trừ sâu, chất bảo quản, chất cấm trong các mẫu thực phẩm, dƣợc liệu, môi trƣờng...
Ngoài ra sắc ký lỏng khối phổ còn đƣợc sử dụng để xác định mức độ tinh khiết của
chất chuẩn hoặc mẫu chuẩn cần phân tích.
1.2.3. Phƣơng pháp xử lý mẫu bằng kỹ thuật chiết pha rắn
Mẫu nƣớc thải từ các công ty sản xuất dƣợc phẩm thƣờng có thành phần rất
phức tạp, hàm lƣợng chất cần phân tích thấp, khó phân tích trực tiếp trên hệ sắc ký.
Vì vậy cần làm giàu mẫu trƣớc khi phân tích, dựa trên các mối liên hệ giữa độ chọn
lọc, độc tính dung môi, giá thành, thời gian... để chọn phƣơng pháp chiết mẫu sao
cho hiệu quả nhất.
Các phƣơng pháp chiết mẫu dùng trong nƣớc thải thông thƣờng là: chiết lỏng lỏng và chiết pha rắn (SPE), trong đó chiết pha rắn đƣợc lựa chọn phổ biến hơn do
những ƣu điểm của nó.
SPE là phƣơng pháp chiết dựa vào sự phân tán của chất phân tích giữa hai pha
lỏng và rắn, trong đó các chất đƣợc chiết từ pha lỏng vào pha rắn. Pha rắn thƣờng là
các hạt nhỏ, xốp đƣợc nhồi vào các ống nhỏ. Pha lỏng chảy qua ống, các chất phân
tích tƣơng tác với pha rắn sẽ đƣợc giữ lại trên ống. Các chất này đƣợc rửa giải khỏi
pha rắn bằng một dung môi khác phù hợp. Thông thƣờng thể tích dung môi rửa giải
nhỏ hơn nhiều so với thể tích dung dịch mẫu. Vì thế chiết pha rắn ngoài tác dụng
làm sạch có thể thực hiện thêm bƣớc làm giàu mẫu. Nguyên liệu tạo pha rắn trong
SPE tƣơng tự nhƣ trong sắc ký lỏng, có thể là dẫn chất polysiloxan, polymer tạo pha
liên kết, ngoài ra còn có cả pha không liên kết.
a) Cơ chế tách chất phân tích khỏi mẫu
14
- Các tạp chất đƣợc rửa giải khỏi cột, chất phân tích đƣợc lƣu giữ lại sao cho
lƣợng tạp chất trong chất phân tích đƣợc giảm thiểu tối đa, chất phân tích sau đó
đƣợc rửa giải bằng một dung môi rửa giải, bay hơi tới cắn hoặc trực tiếp đem đi
phân tích.
- Tạp chất đƣợc giữ lại trên cột, chất phân tích đi ra theo pha lỏng đƣợc thu hồi.
b Các bước trong quy trình chiết pha rắn
Chọn pha rắn: tuỳ theo bản chất của chất phân tích mà lựa chọn pha rắn có bản
chất thích hợp. Mặt khác, tuỳ thuộc vào lƣợng chất phân tích trong mẫu để lựa chọn
cột có lƣợng pha rắn và thể tích rửa giải khác nhau.
Quy trình chiết (SPE cột pha đảo) gồm 4 giai đoạn:
Giai đoạn 1: Hoạt hóa cột chiết. Cho dung môi phù hợp đi qua pha rắn để hoạt
hóa các nhóm hoạt động, loại bỏ các khí trong cột.
Giai đoạn 2: Nạp mẫu. Trƣớc khi nạp, xử lý mẫu sơ bộ để đƣa mẫu vào môi
trƣờng sao cho lƣu giữ đƣợc nhiều nhất chất phân tích trên cột, các tạp chất đi ra
khỏi cột càng nhiều càng tốt tránh cạnh tranh và ảnh hƣởng đến quá trình tƣơng tác
của chất phân tích với pha tĩnh.
Giai đoạn 3: Rửa tạp chất. Sau khi nạp mẫu, trên cột vẫn còn nhiều tạp chất
khác có liên kết với pha tĩnh. Phải chọn đƣợc dung môi rửa tạp sao cho có thể hòa
tan và kéo đƣợc các tạp chất mà không kéo theo chất phân tích.
Giai đoạn 4: Rửa giải. Chất phân tích lƣu giữ trên cột đƣợc hòa tan và kéo ra
khỏi cột bằng một dung môi phù hợp. Cần tối ƣu loại dung môi, thể tích, pH dung
môi rửa giải, tốc độ rửa giải… để có thể rửa giải đƣợc tối đa chất phân tích và rửa
giải tối thiểu các tạp chất còn trên cột [3], [13].
SPE là kỹ thuật có khả năng chiết chất phân tích hiệu quả hơn, dung môi sử
dụng ít, dễ dàng tập trung chất phân tích, kỹ thuật tiến hành thuận tiện, khả năng
làm giàu mẫu tốt, là cơ chế chiết đa dạng phù hợp với chất phân tích, tính chọn lọc
tốt hơn. Tuy nhiên phƣơng pháp có nhƣợc điểm là giá thành còn cao, khó áp dụng ở
quy mô rộng.
15
1.3. MỘT SỐ ĐỀ TÀI NGHIÊN CỨU ĐỊNH LƢỢNG CLINDAMYCIN VÀ
LINCOMYCIN TRÊN THẾ GIỚI
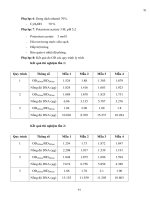
ảng 1.1. Một số nghiên cứu định lượng kháng sinh lincomycin và clindamycin
sử dụng LC- S/ S trên thế giới.
Tài
liệu
[28]
[21]
Hoạt
chất/nền
mẫu
CLI/ huyết
tƣơng
ngƣời
CLI/ huyết
tƣơng động
vật
Điều kiện LC
Điều kiện MS
Khoảng
tuyến tính
LOD
LOQ
- Cột Agilent LC-18
(33x4,6mm; 3µm)
- Pha động: hỗn hợp
methanol/nƣớc/acid formic
với tỉ lệ 90:10:0,05;
- Tốc độ dòng pha động là
4ml/phút
- ESI-MS/MS
- Nhiệt độ nguồn
phun ion: 300oC
- Nebulizer: 40
psi
- Hiệu điện thế
nguồn phun ion:
5,5 kV
- Ion mẹ có m/z
= 426,0
- Ion con có m/z
= 126,0
- ESI-MS/MS
- Ion mẹ có m/z
= 425,3
- Ion con có m/z
= 126,3
- Khoảng
tuyến tính
0,05-3,2µg
/ml
- Hệ số
tƣơng quan r
= 0,9993
- LOD =
0,015
µg /ml
- Khoảng
tuyến tính
0,0520µg/ml
- Hệ số
tƣơng quan r
> 0,998
- LOQ =
0.05µg/ml,
- LOD =
1,3ng/ml
- ESI-MS/MS
- Nhiệt độ nguồn
phun ion: 300oC
- Nebulizer: 40
psi
- Hiệu điện thế
nguồn phun ion:
3 kV
- Ion mẹ có m/z
= 407,0
- Ion con có m/z
= 126,0
- Cột Synergi Hydro-RP - ESI-MS/MS
- Khoảng
tuyến tính 5500 ng/g thịt
và sữa với
- Hệ số
tƣơng quan r
> 0,996.
- LODLIN =
5µg/kg sữa
và 10µg/kg
thịt.
- LOQLIN =
10µg/kg
sữa và
15µg/kg
thịt
- Khoảng
- LOD =
- Cột RP-18 Hypersil (5µm,
100mm×3mm) phối hợp
với cột (25 mm×3mm)
- Pha động: kênh A 0.01M
ammonium
acetat
trong
nƣớc; kênh B là acetonitril
(chạy gradient nồng độ)
- Tốc độ dòng 0,2 ml/phút
[22]
LIN/ thịt và
sữa
[18]
LIN/ mật
- Cột Discovery HS C18
(3µm;15cm×2,1mm).
- Pha động: kênh A nƣớc
loại ion với acid formic
0,1%, kênh B acetonitril
với acid formic 0,1%.
(Chạy gradient nồng độ)
- Tốc độ dòng 0,25ml/phút
- Nhiệt độ cột sắc ký là
25oC.
16
ong
[23]
[35]
LIN/thịt gia
cầm, trứng
và sữa
LIN/thuốc
[36]
CLI/huyết
tƣơng
[30]
LIN/thịt,
gan,
thận lợn
(150×2,0mm; 4µm).
- Pha động kênh A là nƣớc
có
ammonium
acetat
0,01M;
kênh
B
là
acetonitril.
- Tốc độ dòng pha động là
0,25ml/phút. Chạy gradient
nồng độ.
- Cột Capcell Pak C18 (5
µm, 2,0 mm×150 mm)
- Nhiệt độ 40oC.
- Pha động (A) 10mM
ammonium format 0,1%
acid formic trong nƣớc và
(B)
methanol
(chạy
gradient).
- Tốc độ dòng 0,3ml/phút
- Cột Eclipse Plus C18
(50mm×4,6 mm, 1,8µm).
- Nhiệt độ 25oC.
- Pha động (A) nƣớc, acid
triflouroacetic 0,05%, NH3
điều chỉnh pH 3 (B)
acetonitril.
- Chạy đẳng dòng tỉ lệ A:B
90:10.
- Tốc độ dòng 0,5mL/phút
- Cột Hypersil C18
(50mm×4,6mm, 5µm).
- Nhiệt độ 25oC.
- Pha động: acetonitril :
nƣớc : acid triflouroacetic
80:20:0,01. Chạy đẳng
dòng.
- Tốc độ dòng 0,8ml/phút
- Cột Hypersil BDS C18
(5µm, 2,1mm×250mm)
- Nhiệt độ 25oC.
- Pha động (A) amonium
- Ion mẹ có m/z
= 407,0
- Ion con có m/z
= 126,0 và 358,9.
tuyến tính
0,102,0µg/kg
- Hệ số
tƣơng quan r
> 0,999
0,03 µg/kg
- ESI-MS/MS
- Nhiệt độ nguồn
phun ion: 450oC
- Nebulizer: 20
psi
- Hiệu điện thế
nguồn phun ion:
5,5 kV
- Ion mẹ có m/z
= 407,0
- Ion con có m/z
= 126,0 và 359
- ESI-MS/MS
- Nhiệt độ nguồn
phun ion: 325oC
- Nebulizer: 60
psi
- Hiệu điện thế
nguồn phun ion:
2 kV
- Ion mẹ có m/z
= 407,3
- Ion con có m/z
= 126,3 và 359,3
- ESI-MS/MS
- Ion mẹ có m/z
= 425,0
- Ion con có m/z
= 126,0
- Khoảng
tuyến tính
25-250 µg/l
- Hệ số
- LOD =
0,6ng/g. LOQ =
2ng/g
- Khoảng
tuyến tính
0,0520,0µg/ml
- Hệ số
tƣơng quan r
= 0,998
- LOD =
0,015µg/
ml.
- LOQ =
0,05µg /ml
- ESI-MS/MS
- Nhiệt độ nguồn
phun ion: 500oC
- Nebulizer: 40
- Khoảng
tuyến tính 01000µg/kg
thịt và 0-
- LOD =
0,61,5µg/kg
- LOQ =
tƣơng quan
r>0,99
- Khoảng
tuyến tính
10,00100,00µg/ml
- Hệ số
- LOD =
4,21ng/ml.
- LOQ =
14,03ng/ml
tƣơng quan r
= 0,9999
17
formate:formic
acid:
acetonitril
:
nƣớc
,
1:5:50:950; (B) acetonitril
(0,1% acid formic). Chạy
gradient nồng độ.
- Tốc độ dòng 0,2 ml/phút
[20]
[33]
[29]
CLI/ huyết
tƣơng và
nƣớc bọt
LIN/ mật
ong
LIN/ mô
động vật và
sữa bò
psi
- Hiệu điện thế
nguồn phun ion:
5kV
- Ion mẹ có m/z
= 407,2
- Ion con có m/z
= 126,1 và 359,2
- Cột Agilent Zorbax SB- - Ion mẹ có m/z
C18 (3,5 µm, 21 mm×30 = 425,1
mm)
- Ion con có m/z
o
- Nhiệt độ 50 C.
= 126,1
- Pha động methanol : nƣớc
:
acid
triflouracetic
40:60:0,01
- Tốc độ dòng 0,6 ml/phút
- Cột Zorbax C18 (5µm, - APCI-MS/MS
2,1mm×150mm), cột bảo - Nhiệt độ nguồn
vệ C8 (4mm × 2,0mm)
phun ion: 550oC
- Pha động (A) methanol - Tốc độ khí
(B)
acetonitril,
acid phun: 90-175l/h
triflouroacetic 0,1% (C) - Ion mẹ có m/z
nƣớc, acid triflouroacetic = 407,2
0,1%.
Tỉ
lệ
A:B:C - Ion con có m/z
10:22,5:67,5 sau đó 7 phút = 126,1
chuyển sang 10:90:0.
- Tốc độ dòng 0,5 ml/phút
- Cột Hypersil C18 (5µm, - ESI-MS/MS
2,1mm×250mm) và cột bảo - Nhiệt độ nguồn
vệ C18 (7,5mm, 4,6mm)
phun ion: 500oC
o
- Nhiệt độ 25 C.
-Nebulizer: 40psi
- Pha động (A) acetonitril, - Hiệu điện thế
acid triflouroacetic 0,1% nguồn phun ion:
(B) ammonium format : 5kV
formic acid : acetonitril : - Ion mẹ có m/z
nƣớc, 1:5:50:950. A:B 3:7
= 407,2
- Tốc độ dòng 0,2 ml/phút
- Ion con có m/z
= 126,1 và 359,2
3000 µg/kg
gan hoặc
thận
- Hệ số
tƣơng quan r
= 0,9990
đến 0,9999
25-50
µg/kg
- Khoảng
tuyến tính
0,05 –
0,15µg/ml
- Hệ số
tƣơng quan r
= 0,991
- LOD =
0,03ng/ml.
- LOQ =
10ng/ml
- Khoảng
tuyến tính
0,0550µg/ml
- Hệ số
tƣơng quan r
= 0,9996
- LOD =
0,007µg/g
- Khoảng
tuyến tính
253000µg/kg
- Hệ số
tƣơng quan r
= 0,995
- LOD =
1,5-8,8
µg/kg
- LOQ =
25-50
µg/kg