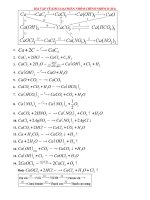PHÂN NHÓM IIIA pptx
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (259.37 KB, 22 trang )
12/7/2010
604001 - chương 7
1
CHƯƠNG 7 – PHÂN NHÓM IIIA
I. NHẬN XÉT CHUNG
II. CÁC ĐƠN CHẤT
III.CÁC HỢP CHẤT CÓ SỐ OXIHOA DƯƠNG +3
12/7/2010
604001 - chương 7
2
I. NHẬN XÉT CHUNG
• Phân nhóm IIIA gồm có: B, Al, Ga, In, Tl
•Cấu hình electron hóa trò:
ns
2
np
1
3
-3e
0
X X
-
+
⎯→⎯
Tính khử mạnh
• B là PK , các nguyên tố còn lại là KL
•Ga Tl
(+1) ↑ và (+3) ↓
12/7/2010
604001 - chương 7
3
1.Bo
•Tính chất lý, hóa học:
- B tồn tại ở một số dạng thù hình bền. Có hai dạng:
vô đònh hình và tinh thể.
- B là chất bán dẫn, độ dẫn điện tăng lên khi thay đổi
nhiệt độ.
- Khó nóng chảy.
-Về mặt hóa học có tính chất giống Si:
+ Bền ở điều kiện thường, chỉ tác dụng trực tiếp với
flo
+ ở nhiệt độ cao thể hiện tính khử.
II.CÁC ĐƠN CHẤT
12/7/2010
604001 - chương 7
4
4B(vđh) + 3O
2
Ỉ 2B
2
O
3
; ΔΗ = −1461 kJ/mol
o
298
3SiO
2
+ 4B Ỉ 3Si + 2B
2
O
3
t cao
+ tác dụng với axit có tính oxi hóa mạnh: HNO
3
, H
2
SO
4
,
nước cường toan Ỉ H
3
BO
3
B + HNO
3
+ H
2
O Ỉ H
3
BO
3
+ NO
+ tác dụng với kiềm Ỉ H
2
2B + 2KOH + 2H
2
O Ỉ 2KBO
2
+ 3H
2
+ tác dụng với H
2
Ỉ boran B
2
H
6
, B
4
H
10
…
+ tác dụng với KL Ỉ borua MgB
2
, CrB…
1.Bo
12/7/2010
604001 - chương 7
5
•Điều chế – ứng dụng:
- Dạng tồn tại chủ yếu: H
3
BO
3
và muối Na
2
B
4
O
7
. Khoáng
chủ yếu là: borac Na
2
B
4
O
7
. 10H
2
O
- Phương pháp nhiệt kim loại: dùng Na, Mg khử B
2
O
3
B
2
O
3
+ 3Mg Ỉ 2B + 3MgO
t
- Nhiệt phân boran: B
2
H
6
Ỉ 2B + 3H
2
t
-Ứng dụng: - chế tạo hợp kim thép Ỉ tăng độ cứng
-B hóa bề mặt thép Ỉ tăng độ bền hóa
- vật liệu hãm trong quá trình phản ứng hạt nhân
1.Bo
12/7/2010
604001 - chương 7
6
-là kim loại trắng bạc, khá bền, dai, dễ kéo dài, dát mỏng,
dẫn nhiệt, dẫn điện tốt.
Vềmặthóahọc: Al lànguyêntốrấthoạtđộng
- Ở điều kiện thường bền khi tiếp xúc O
2
không khí
và nước Ỉ lớp Al
2
O
3
bền
-Tác dụng mạnh với PK hoạt động: bốc cháy trong
halogen, khử được nhiều chất như oxyt KL…
-Tan trong axit và kiềm
- Al bò thụ động hóa trong HNO
3
, H
2
SO
4
đặc nguội
2. Nhôm
12/7/2010
604001 - chương 7
7
Điều chế : Điện phân nóng chảy hỗn hợp Al
2
O
3
+
Na
3
AlF
6
ở 950
0
C với điện cực grafit
2. Nhôm
12/7/2010
604001 - chương 7
8
ÖÙng duïng:
12/7/2010
604001 - chương 7
9
III. CÁC HP CHẤT CÓ SỐ OXIHÓA DƯƠNG (+3)
1.Các hợp chất B (+3)
a. Oxyt B
2
O
3
(anhydrit boric)
- Có hai dạng: dạng thủy tinh và dạng tinh thể
- Liên kết B-O-B bền nhiệt nhưng lại dễ bò nước thủy
phân Ỉ hút ẩm mạnh, dễ tan trong nước
(B
2
O
3
)
n
(HBO
2
)
3
H
5
B
3
O
7
H
3
BO
3
a.polimetaboric a.polioctoboric a.boric
+ H
2
O+ H
2
O+ H
2
O
12/7/2010
604001 - chương 7
10
- Khi đun nóng H
3
BO
3
thì xảy ra quá trình ngược lại
B
2
O
3
+ H
2
O
t
0
HBO
2
+ H
2
O
t
0
H
3
BO
3
b.Axit boric và muối borat
-H
3
BO
3
là axit bền nhất trong các axit bo, có cấu trúc lớp
O
O
O
O
O
O
HH
H
H
H
H
O
O
O
O
O
O
HH
H
H
H
H
B
B
O
O
O
O
O
O
HH
H
H
H
H
O
H
B
O
O
B
O
H
B
B
1.Các hợp chất B (+3)
12/7/2010
604001 - chương 7
11
-Kết tinh dạng vảy cá, không màu, tan ít trong nước lạnh,
tan nhiều trong nước nóng
-Là axit yếu K
1
= 6.10
-10
-Tác dụng với kiềm dư Ỉ muối borat nghèo nước
3H
3
BO
3
+ 3NaOH Ỉ (NaBO
2
)
3
+ 6H
2
O
4H
3
BO
3
+ 2NaOH Ỉ Na
2
B
4
O
7
+ 6H
2
O
- Muối borat + axit Ỉ H
3
BO
3
Na
2
B
4
O
7
+ H
2
SO
4
+ 5H
2
O Ỉ 4H
3
BO
3
+ Na
2
SO
4
1.Các hợp chất B (+3)
12/7/2010
604001 - chương 7
12
- Các borat có cấu trúc polime. Quan trọng là muối
natri tetraborat Na
2
B
4
O
7
.10H
2
O
O
O
O
B
O
O
B
O
B
O
O
B
O
O
B
O
B
O
O
O
B
B
Na
+
Na
+
Na
+
Na
+
-Borac(Na
2
B
4
O
7
.10H
2
O) là tinh thể không màu, tan ít
trong nước. Khi tan trong nước bò thủy phân:
Na
2
B
4
O
7
+7 H
2
O ⇔ 4H
3
BO
3
+ 2 NaOH
1.Các hợp chất B (+3)
12/7/2010
604001 - chương 7
13
-Các borat, oxyt B
2
O
3,
và axit H
3
BO
3
khi nóng chảy
hòa tan các oxyt kim loại Ỉ tạo thành ngọc borat
có màu đặc trưng của kim loại
Na
2
B
4
O
7
+ CoO Ỉ 2NaBO
2
.Co(BO
2
)
2
ngọc borat coban màu
xanh biển
1.Các hợp chất B (+3)
12/7/2010
604001 - chương 7
14
2.Các hợp chất Al(+3)
a.Oxyt Al
2
O
3
-Tồn tại dưới một số dạng đa hình Ỉ dạng bền α-Al
2
O
3
và
γ-Al
2
O
3
-Dạng α-Al
2
O
3
có độ bền nhiệt cao, không tan trong nước,
không tác dụng với axit và kiềm
-α-Al
2
O
3
chỉ phản ứng khi nấu chảy với kiềm hay K
2
S
2
O
7
Al
2
O
3
+ 2NaOH Ỉ 2NaAlO
2
+ H
2
O
Al
2
O
3
+ 3K
2
S
2
O
7
Ỉ Al
2
(SO
4
)
3
+ 3K
2
SO
4
12/7/2010
604001 - chương 7
15
- α-Al
2
O
3
được tạo thành khi nung Al(OH)
3
trên 1000
0
C.
- α-Al
2
O
3
còn tồn tại trong thiên nhiên dưới dạng khoáng
corundum.
-γ-Al
2
O
3
được tạo thành khi nung Al(OH)
3
ở nhiệt độ thấp dưới
500
0
C
-Ở khoảng 1000
0
C dạng γ-Al
2
O
3
chuyển sang dạng α
-γ-Al
2
O
3
hoạt động hơn, tan trong các dung dòch kiềm, axit thể
hiện tính lưỡng tính của Al
2
O
3
Al
2
O
3
+ 6NaOH + 3H
2
O Ỉ 2Na
3
[Al(OH)
6
]
3Al
2
O
3
+ 3H
2
SO
4
+ 9H
2
O Ỉ [Al(H
2
O)
6
]
2
(SO
4
)
3
2.Các hợp chất Al(+3)
12/7/2010
604001 - chương 7
16
Điều chế:
Trong CN
: Sản xuất từ boxit theo quy trình Baye:
boxit
Dd NaOH nóng
Natri aluminat
Thủy phân
Al(OH)
3
t
0
Al
2
O
3
Trong PTN: Nhiệt phân Al(OH)
3
Ứng dụng: (tựđọc)
2.Các hợp chất Al(+3)
12/7/2010
604001 - chương 7
17
Quy trình Bayer sảnxuấtAl từ quặng bauxite
12/7/2010
604001 - chương 7
18
12/7/2010
604001 - chương 7
19
b.Hydroxyt Al(OH)
3
- Có các dạng đa hình bền: hydraghilit (gipxit) Al
2
O
3
.3H
2
O và
bơmit, diaspo Al
2
O
3
.H
2
O hay AlOOH
A l A l A l
O O
O O
H O H
2
H OH
2
HOH H OH
2
OH
2
OH
2
HO OH
A l A l A l
O O
O O
H H O H
2
H H O H
2
H O O H H O O H
2.Các hợp chất Al(+3)
12/7/2010
604001 - chương 7
20
-Al(OH)
3
được tạo thành : Al
3+
+ 3OH
-
= Al(OH)
3
↓ kết tủa
keo nhầy .
-có thành phần Al
2
O
3
.nH
2
O Ỉ Al(OH)
3
Ỉ Al
2
O
3
- Al(OH)
3
là hợp chất lưỡng tính : có tính axit và bazơ
Al(OH)
3
+ 3NaOH Ỉ Na
3
[Al(OH)
6
]
Al(OH)
3
+ NaOH Ỉ Na[Al(OH)
4
]
Al(OH)
3
+ 3HCl + 3H
2
O Ỉ [Al(H
2
O)
6
]Cl
3
Al(OH)
3
+ 3HCl Ỉ AlCl
3
+ 3H
2
O
-Nấu chảy kiềm với Al(OH)
3
Al(OH)
3
+ KOH Ỉ KAlO
2
+ 2H
2
O
2.Các hợp chất Al(+3)
12/7/2010
604001 - chương 7
21
-Tính lưỡng tính của Al(OH)
3
được thể hiện trong cân bằng
H
3
O
+
[Al(H
2
O)
6
]
3+
Al(OH)
3
[Al(OH)
6
]
3−
H
3
O
+
OH
-
OH
-
c.Muối Al
3+
-MuốiAl
3+
dễ tan và bò thủy phân mạnh
[Al(H
2
O)
6
]
3+
[Al(H
2
O)
5
OH]
-
+ H
+
Al
2
S
3
+ 6H
2
O Ỉ 2Al(OH)
3
↓ + 3H
2
S↑
-Nhôm sunfat kết hợp với sunfat kiềm tạo thành
M
2
Al
2
(SO
4
)
3
.24H
2
O (phèn nhôm)
2.Các hợp chất Al(+3)
12/7/2010
604001 - chương 7
22
Hòatan hoàntoàn5,1 g Al
2
O
3
bằng dung dòch chứa
0,06 mol Ba(OH)
2
. Tính thể tích dung dòch H
2
SO
4
2M
cần thêm vào dung dòch thu được đề toàn bộ ion
aluminat có trong dung dòch chuyển thành kết tủa.
Tính khối lượng kết tủa tạo thành.
BÀI TẬP